| Japanese top page / English top page |
PAICS
Parallelized ab initio Calculation System based on FMO
|
|
|||
|
|
|||
| 惓忢宆僾儕僆儞僞儞僷僋幙偵娭偟偰丄巆婎亅巆婎娫憡屳嶌梡偍傛傃巆婎亅梟攠暘巕娫憡屳嶌梡傪夝愅偟偨椺傪丄偙傟傑偱偺僾儗僛儞偱巊梡偟偨帒椏傪梡偄偰愢柧偟傑偡丅傑偨丄偙偙偱徯夘偟偰偄傞寁嶼偼榑暥偲偟偰弌斉偝傟偰偍傝傑偡偺偱 [1] 丄徻嵶偼偦偪傜傪嶲徠偟偰壓偝偄丅 | |||
|
捠忢丄検巕壔妛寁嶼偱偼丄尨巕妀偺埵抲傪屌掕偟丄揹巕偺塣摦曽掱幃乮僔儏儗乕僨傿儞僈乕曽掱幃乯傪夝偒傑偡丅傛偭偰丄検巕壔妛寁嶼偱僞儞僷僋幙偺峔憿曄壔傪捈愙僔儈儏儗乕僔儑儞偡傞偙偲偼崲擄偱偡丅偟偐偟丄僾儕僆儞昦偺尨場偼惓忢宆偐傜堎忢宆傊偺僐儞僼僅乕儊乕僔儑儞曄壔側偺偱丄偙偺峔憿曄壔偺僾儘僙僗傪挷傋傞偙偲偼廳梫側尋媶壽戣偱偡丅偦偙偱丄僐儞僼僅乕儊乕僔儑儞曄壔偵娭楢偡傞忣曬傪摼傞偨傔偵丄惓忢宆僾儕僆儞僞儞僷僋幙偵娭偟偰FMO寁嶼 [2] 傪幚峴偟傑偟偨丅
嬶懱揑偵偼丄惓忢宆僾儕僆儞僞儞僷僋幙偵梟攠暘巕壛偊偨儌僨儖宯傪嶌惉偟丄FMO寁嶼傪幚峴偟丄巆婎亅巆婎娫憡屳嶌梡僄僱儖僊乕偲巆婎亅梟攠暘巕娫憡屳嶌梡僄僱儖僊乕傪丄僼儔僌儊儞僩娫憡屳嶌梡僄僱儖僊乕乮IFIE乯 [3] 偐傜嶼弌偟傑偟偨丅偙傟傜傪夝愅偡傞偙偲偱丄惓忢宆偺峔憿堐帩偵廳梫偵婑梌偡傞憡屳嶌梡傪摿掕偟丄堎忢宆傊偺僐儞僼僅乕儊乕僔儑儞曄壔偵娭楢偡傞忣曬傪摼傛偆偲帋傒傑偟偨丅 |
|||
 |
|||
| 傑偢丄PDB傪弶婜峔憿偲偟丄屆揟揑側暘巕摦椡妛寁嶼偺僩儔僕僃僋僩儕乕偐傜儔儞僟儉偵40揰偺峔憿傪敳偒弌偟傑偟偨丅偦偙偐傜8侌埲忋棧傟偨梟攠暘巕傪庢傝彍偒儌僨儖峔憿乮壓恾嶲徠乯偲偟丄偙傟傜偵娭偟偰FMO寁嶼傪幚峴偟丄巆婎亅巆婎娫憡屳嶌梡偍傛傃巆婎亅梟攠娫憡屳嶌梡偺夝愅傪峴偄傑偟偨丅寁嶼偵偼RI-MP2朄傪梡偄丄婎掙娭悢偵偼cc-pVDZ傪巊偄傑偟偨丅 | |||
 |
|||
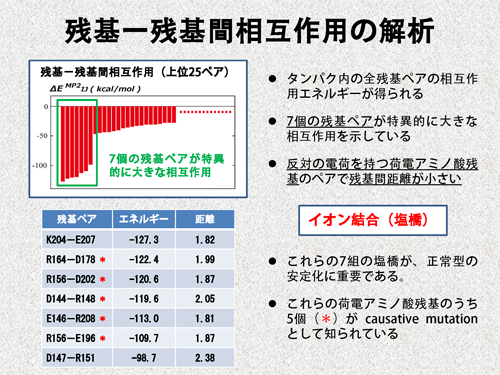
| 偦傟偱偼丄寁嶼寢壥傪尒偰傒傑偟傚偆丅嵟弶偵丄巆婎亅巆婎娫憡屳嶌梡僄僱儖僊乕傪夝愅偟傑偡丅埲壓偺僌儔僼偵偼丄嵟傕憡屳嶌梡僄僱儖僊乕偑戝偒偐偭偨25慻偺巆婎儁傾偺僄僱儖僊乕偑僾儘僢僩偝傟偰偄傑偡丅偙傟傪尒傞偲丄7慻偺儁傾偑摿堎揑偵戝偒側憡屳嶌梡僄僱儖僊乕傪帵偟偰偄傞偙偲偑暘偐傝傑偡丅偦偟偰丄偙傟傜偺儁傾偼丄屳偄偵斀懳偺揹壸傪帩偭偨壸揹傾儈僲巁巆婎偱偁傝丄巆婎娫嫍棧傕旕忢偵彫偝偄偙偲偑暘偐傝傑偡乮昞傪嶲徠乯丅廬偭偰丄僀僆儞寢崌乮墫嫶乯傪宍惉偟偰偄傞偲峫偊傜傟丄偙偺7慻偺墫嫶偑惓忢宆僾儕僆儞僞儞僷僋幙偺埨掕壔偵廳梫偵婑梌偟偰偄傞偲悇應偱偒傑偡丅傑偨丄7慻偺偆偪5慻偺墫嫶傪宍惉偡傞巆婎偼丄昦尨惈偺儈儏乕僥乕僔儑儞乮昦婥偑婲偙傝傗偡偔側傞儈儏乕僥乕僔儑儞乯偲偟偰抦傜傟偰偍傝丄偙傟傜偺墫嫶偑惓忢宆偺埨掕壔偵廳梫偱偁傞偙偲偄偆悇應偲柕弬偟傑偣傫丅 | |||
 |
|||
|
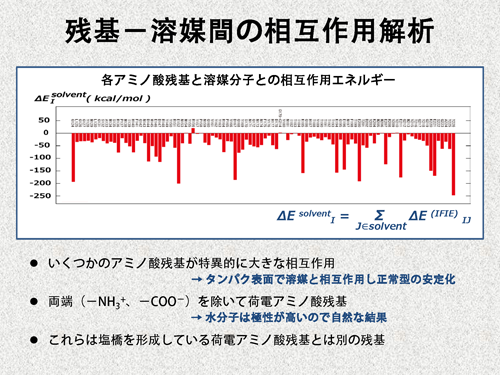
師偵丄巆婎亅梟攠暘巕娫憡屳嶌梡僄僱儖僊乕偵拲栚偟傑偡丅偄偔偮偐偺傾儈僲巁巆婎偑梟攠暘巕偲摿堎揑偵戝偒側憡屳嶌梡僄僱儖僊乕傪帵偟偰偄傞偙偲偑暘偐傝傑偡丅偙傟傜偺巆婎偼丄梟攠暘巕偲憡屳嶌梡偡傞偙偲偱丄惓忢宆偺峔憿堐帩偵婑梌偟偰偄傞偲峫偊傜傟傑偡丅徻偟偔尒偰傒傞偲丄椉枛抂偺巆婎傪彍偒丄慡偰壸揹傾儈僲巁巆婎偱偁傞偙偲偑暘偐傝傑偡乮椉枛抂偼廔抂張棟偲偟偰揹壸傪帩偭偰偄傞乯丅偙傟偼丄悈暘巕偑崅偄嬌惈傪傕偭偰偄傞偨傔摉慠偺寢壥偲偄偊傑偡丅
偙偙偱廳梫側偺偼丄梟攠暘巕偲戝偒側憡屳嶌梡僄僱儖僊乕傪壱偄偱傞壸揹傾儈僲巁巆婎偼丄墫嫶傪宍惉偟偰偄傞壸揹傾儈僲巁巆婎偲偼暿偺巆婎偱偁傞偲偄偆偙偲偱偡丅偮傑傝丄壸揹傾儈僲巁巆婎偼丄乽墫嫶傪宍惉偡傞栶妱乿偐乽梟攠偲憡屳嶌梡偡傞栶妱乿偺偳偪傜偐堦曽傪捠偠偰丄惓忢宆偺峔憿堐帩偵婑梌偟偰偄傞偲偄偆偙偲偵側傝傑偡丅崱夞偺椺偱偼丄22屄偺壸揹傾儈僲巁巆婎偺偆偪丄13屄偑墫嫶傪宍惉偟丄巆傝偺9屄偑梟攠暘巕偲嫮偔憡屳嶌梡偟偰偄傑偟偨丅偦偟偰丄偙傟傜偺堘偄偼丄寁嶼偝傟偨憡屳嶌梡僄僱儖僊乕偐傜柧妋偵嬫暿偱偒傑偟偨丅 偙偙偱彮偟堦斒揑側媍榑傪偡傞偲 . . . 僞儞僷僋幙偼丄僄僱儖僊乕揑偵嵟傕桳棙側峔憿傪僱僀僥傿僽峔憿偲偟偰慖戰偟偰偄傞偼偢偱偡丅椺偊偽丄崱夞偺惓忢宆僾儕僆儞僞儞僷僋幙偱偼丄K204偲E207偑墫嫶傪宍惉偟偰偄傑偟偨乮忋偺昞嶲徠乯丅偟偐偟丄偙傟傜偑墫嫶傪嶌傜偢丄僞儞僷僋昞柺偵撍偒弌偰梟攠偲憡屳嶌梡偡傞傛偆側峔憿傕丄僞儞僷僋偺僐儞僼僅乕儊乕僔儑儞嬻娫偵偼懡悢懚嵼偡傞偼偢偱偡丅偦傟偱傕丄K204偲E207偑墫嫶傪宍惉偡傞峔憿偑僱僀僥傿僽峔憿側偺偼丄 偦偺峔憿偑僄僱儖僊乕揑偵嵟傕桳棙偩偐傜偱偡丅偮傑傝丄K204傗E207偑丄梟攠暘巕偲憡屳嶌梡偡傞栶妱偱偼側偔墫嫶傪宍惉偡傞栶妱傪帩偭偰偄傞偺偵偼丄僄僱儖僊乕揑側昁慠惈偑偁傞偐傜偱偡丅 偙偙偱偼丄惓忢宆僾儕僆儞僞儞僷僋幙偺壸揹傾儈僲巁巆婎偺傒偵拲栚偟傑偟偨偑丄條乆側僞儞僷僋幙偵娭偟偰丄乽奺巆婎偑僱僀僥傿僽峔憿偺埨掕壔偵壥偨偡栶妱乿傪栐梾揑偵挷傋傞偙偲偑偱偒傟偽丄僞儞僷僋幙偺崅師峔憿宍惉偺儊僇僯僘儉偵娭楢偡傞柺敀偄尋媶偑偱偒傞偺偱偼側偄偐偲巚偄傑偡丅傕偪傠傫丄崅師峔憿偺宍惉偵偼僄儞僩儘僺乕揑側岠壥傕廳梫偱丄憡屳嶌梡僄僱儖僊乕乮偮傑傝丄僄儞僞儖僺乕揑側岠壥乯偩偗偱慡偑棟夝偱偒傞偲偼巚偄傑偣傫丅偑丄FMO朄傪墳梡偡傞壜擻惈偺1偮偱偁傞偲巚偄傑偡丅 |
|||
 |
|||
|
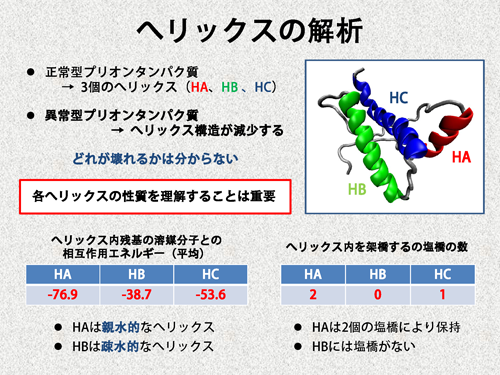
崱搙偼丄奺傊儕僢僋僗偛偲偵憡屳嶌梡傪尒偰傒傑偟傚偆丅惓忢宆僾儕僆儞僞儞僷僋幙偵偼3偮偺傊儕僢僋僗偑懚嵼偟傑偡乮AH丄HB丄HC乯丅偦偟偰丄堎忢宆傊曄壔偡傞偲丄傊儕僢僋僗峔憿偺堦晹偑徚幐偡傞偙偲偑抦傜傟偰偄傑偡丅偟偐偟丄偳偺傊儕僢僋僗峔憿偑夡傟傞偺偐偼暘偐偭偰偍傜偢丄偦傟傪撍偒巭傔傞偙偲偑偱偒傟偽丄僾儕僆儞尋媶偵偍偗傞戝偒側恑揥偲側傝傑偡丅傕偪傠傫丄惓忢宆僾儕僆儞僞儞僷僋幙偺検巕壔妛寁嶼偺傒偐傜丄夡傟傞傊儕僢僋僗傪梊應偡傞偙偲偼偱偒傑偣傫偑丄乽奺傊儕僢僋僗偺惈幙乿傪媍榑偡傞偙偲偼壜擻偱偡丅
椺偊偽丄奺傊儕僢僋僗偵娷傑傟傞傾儈僲巁巆婎偺梟攠暘巕偲偺憡屳嶌梡僄僱儖僊乕偺暯嬒抣偼丄HA偑嵟傕戝偒偔HB偑嵟傕彫偝偔側傝傑偟偨乮昞傪嶲徠乯丅廬偭偰丄HA偼恊悈揑惈幙傪帩偭偨傊儕僢僋僗偱偁傝丄HB偼慳悈揑惈幙傪帩偭偨傊儕僢僋僗偱偁傞偲尵偊傑偡丅傑偨丄崱夞偺寁嶼偱摿掕偝傟偨7屄偺墫嫶偺偆偪丄2屄偑HA撪偵懚嵼偡傞偺偵懳偟偰丄HB偵偼偦偺傛偆側墫嫶偑懚嵼偟傑偣傫丅廬偭偰丄HA偺傊儕僢僋僗峔憿偼僀僆儞揑側憡屳嶌梡偵傛傝嫮屌偵曐偨傟偰偄傞堦曽偱丄HB偺傊儕僢僋僗峔憿偼僀僆儞寢崌偲偄偆堄枴偱偼庛偄偲悇應偱偒傑偡丅 |
|||
 |
|||
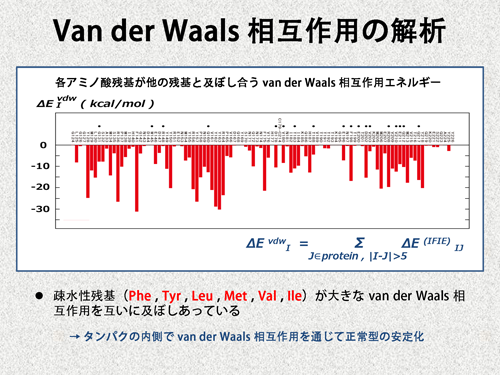
| 師偼丄van der Waals 憡屳嶌梡偵拲栚偟傑偡丅検巕壔妛寁嶼偱偼丄van der Waals 憡屳嶌梡偼揹巕憡娭偲偟偰屄暿偵寁嶼偝傟傞偺偱丄van der Waals 憡屳嶌梡偩偗傪敳偒弌偟偨夝愅偑壜擻偲側傝傑偡丅埲壓偵帵偟偨偺偼丄奺傾儈僲巁巆婎偑帺暘埲奜偺傾儈僲巁巆婎偲媦傏偡van der Waals 憡屳嶌梡僄僱儖僊乕偱偡丅偙傟傪尒傞偲丄慳悈惈巆婎偑斾妑揑戝偒側憡屳嶌梡傪帵偟偰偄傞偙偲偑暘偐傝傑偡丅偙傟偼丄僞儞僷僋幙壢妛偺堦斒揑側峫偊曽丄偮傑傝丄乽恊悈惈巆婎偼僞儞僷僋昞柺偱梟攠暘巕偲憡屳嶌梡偟丄慳悈惈巆婎偼撪懁偱屳偄偵旕嬌惈偺憡屳嶌梡傪偟偰丄僞儞僷僋幙偺棫懱峔憿偵婑梌偡傞乿偲偄偆尒夝偲丄柕弬偟側偄寢壥偩偲偄偊傑偡丅 | |||
 |
|||
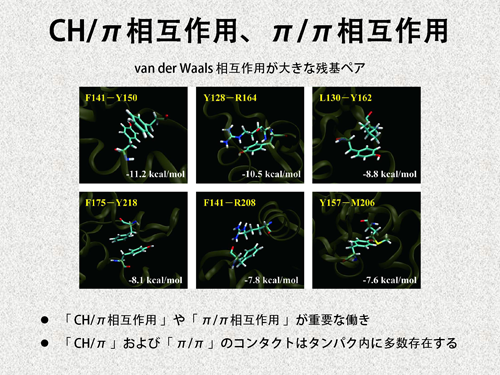
| 嬤擭丄CH/兾憡屳嶌梡傗兾/兾憡屳嶌梡偑丄壔妛偺條乆側応柺偱廳梫側栶妱傪壥偨偟偰偄傞偲峫偊傜傟偰偄傑偡丅埲壓偵丄変乆偺寁嶼偱嵟傕 van der Waals 憡屳嶌梡傪壱偄偱偄偨6屄偺巆婎儁傾傪帵偟傑偡丅偙傟傜偺儁傾偼慡偰CH/兾傕偟偔偼兾/兾憡屳嶌梡傪媦傏偟偁偭偰偄傑偡丅傑偨丄偙偙偵帵偟偨傕偺埲奜偵傕丄悢懡偔偺CH/兾傗兾/兾僐儞僞僋僩偑崅偄憡屳嶌梡僄僱儖僊乕傪帵偟偰偄傑偟偨丅偮傑傝丄変乆偺寁嶼傕丄CH/兾憡屳嶌梡傗兾/兾憡屳嶌梡偑丄僞儞僷僋幙偺棫懱峔憿堐帩偵廳梫側栶妱傪壥偨偟偰偄傞偙偲傪帵嵈偡傞寢壥偲側偭偰偄傑偡丅 | |||
 |
|||
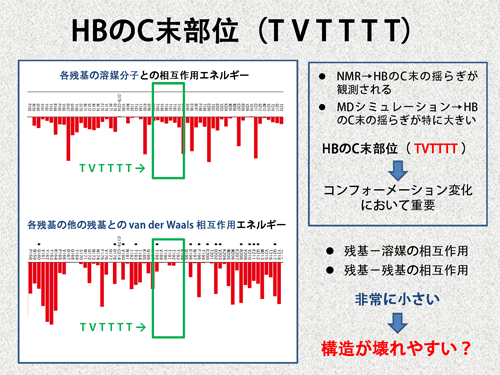
| 嵟屻偵丄HB偺C枛晹埵偵娭偟偰媍榑偟偰傒傑偟傚偆丅嬤擭偺幚尡傗暘巕摦椡妛偺寢壥偐傜丄HB偺C枛晹埵乮摿偵丄TVTTTT偺僗儗僆僯儞偑暲傇晹暘乯偺梙傜偓偑摿堎揑偵戝偒偄丄偮傑傝丄偙偺晹暘偑堎忢宆傊偺峔憿曄壔偱廳梫偱偁傞偲偄偆撪梕偺尋媶偑曬崘偝傟偰偄傑偡丅偦偙偱丄変乆偺寁嶼寢壥傪丄偙偺傛偆側棫応偐傜尒偰傒傞偙偲偵偟傑偟傚偆丅埲壓偵帵偟偨偺偼丄奺巆婎偺梟攠偲偺憡屳嶌梡僄僱儖僊乕偍傛傃懠偺巆婎偲壱偖 van der Waals 憡屳嶌梡僄僱儖僊乕偺TVTTTT晹暘偱偡丅梟攠暘巕偲傕懠偺巆婎偲傕傎偲傫偳憡屳嶌梡傪媦傏偟偰偄側偄偙偲偑暘偐傝傑偡丅偮傑傝丄HB偺C枛偺僗儗僆僯儞偑暲傇晹暘偼丄変乆偺寁嶼偐傜傕峔憿揑偵庛偄偲悇應偡傞偙偲偑偱偒丄忋偺幚尡傗暘巕摦椡妛寁嶼偲柕弬偟側偄寢壥偩偲偄偊傑偡丅 | |||
 |
|||
| 偙傟傑偱FMO朄偼丄僞儞僷僋幙亅掅暘巕壔崌暔傗僞儞僷僋幙亅DNA偲偄偭偨丄惗懱暘巕偺乽暘巕娫憡屳嶌梡夝愅乿偵棙梡偝傟偰棃傑偟偨丅堦曽偱丄偙偙偱徯夘偟偨傛偆側乽暘巕撪憡屳嶌梡夝愅乿偵棙梡偟偨椺偼偁傑傝曬崘偝傟偰偄傑偣傫丅尰嵼丄僞儞僷僋幙壢妛偵偍偄偰丄崅師峔憿偺宍惉偼旕忢偵廳梫偱戝偒側僥乕儅偲偄偊傑偡丅崱屻丄FMO朄偑丄偦偺傛偆側尋媶暘栰偱傕桳岠偵棙梡偝傟傞偙偲傪婜懸偟偰偄傑偡丅 | |||
| [1] | Interaction analysis of the native structure of prion protein with quantum chemical calculations, T. Ishikawa and K. Kuwata, J. Chem. Theor. Comput., 6 (2010) 538-547 (DOI: 10.1021/ct900456v) | ||
| [2] | Fragment molecular orbital method: an approximate computational method for large molecules, K. Kitaura, E. Ikeo, T. Asada, T. Nakano, and M. Uebayasi, Chem. Phys. Lett., 313 (1999) 701-706 (DOI: 10.1016/S0009-2614(99)00874-X) | ||
| [3] | Fragment molecular orbital method: use of approximate electrostatic potential, T. Nakano, T. Kaminuma, T. Sato, K. Fukuzawa, Y. Akiyama, M. Uebayasi, and K. Kitaura, Chem. Phys. Lett., 351 (2002) 475-480 (DOI: 10.1016/S0009-2614(01)01416-6) | ||
|